لکودیستروفی متاکروماتیک
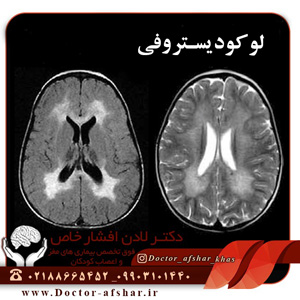
لکودیستروفی متاکرومیک (MLD) که کمبود آریل سولفاتاز A هم خوانده میشود، نوعی بیماری ذخیرهای لیزوزومی است.
علائم بالینی[ویرایش]
- نوع شیرخوارگی دیررس: قبل از ۳۰ ماهگی شروع شده و در عرض ۱ تا ۷ سال منجر به مرگ میشود. اولین تظاهر آن از دست دادن مهارتهای حرکتی اکتسابی بخصوص راه رفتن است. کاهش تونوس عضلانی، ژنو رکرواتوم شدید، کاهش یا غیاب رفلکسهای تاندونی، تأخیر در راه رفتن در برخی از بیماران، بروزعدم تعادل و ضعف بدنبال عفونت که ممکن است ناپدید شده و دوباره بعداً ظاهر شود و درد شدید پاها در بیمار رخ میدهد. در مرحله بعدی، عدم تعادل، دیزآرتری یا عدم تکلم، پسرفت عملکردهای مغزی، افزایش تونوس عضلانی و رفلکسهای تاندونی، نیستاگموس و آتروفی عصب بینایی و گاهی لکه قرمز آلبالویی در ماکولا ظاهر میشوند. سپس بیمار دچار فلج اسپاستیک همه اندامها، رژیدیتی دسربره یا رژیدیتی دکورتیکه، حرکات دیستونیک، تشنج در یک سوم موارد، اشکال در تغذیه و از دست دادن قدرت تکلم میشود. در مرحله آخر عدم پاسخ به والدین و لبخند زدن، از دست دادن ارتباط با محیط اطراف، کوری، عدم توانایی بلع و نیاز به تغذیه با لوله بینی-معدی بروز میکند و مرگ بیمار بدنبال ابتلا به ذات الریه رخ میدهد.
- نوع نوجوانی: بین ۴ تا ۱۶ سالگی با کاهش عملکرد در مدرسه، گاهی رفتار غیر معمول، حالت گیجی، مانس، سایکوز یا بیماری عاطفی، اختلال در راه رفتن، عدم تعادل، رژیدیتی عضلانی و اشکال در وضعیت بدن، عدم راه رفتن، بیاختیاری ادرار، تظاهرات احشایی غیرمعمول نظیر کوله سیستیت حاد، پانکراتیت خونریزی دهنده مزمن، توده شکمی یا خونریزی گوارشی بروز میکند.
- نوع بزرگسالی: پس از بلوغ حدود ۱۵ سالگی و گاهی در ۶۲ سالگی تظاهر میکند. در این نوع علائم روانی، دمانس به صورت از دست دادن حافظه یا کاهش توانایی ذهنی، اسکیزوفرنی، بیثباتی هیجانی، اضطراب یا بی تفاوتی، توهمات شنوایی، هذیان، سایکوز، افسردگی و الکلیسم مزمن مشاهده شدهاست. اشکالات حرکتی به صورت اختلال در راه رفتن و دیزآرتری، کاهش تونوس عضلانی و افزایش
رفلکسهای تاندونی، عدم تعادل و یافتههای مشابه پارکینسون، آسیب اعصاب محیطی در برخی از بیماران، دیستونی، ضعف اسپاستیک همه اندامها، آتروفی عصب بینایی و نیستاگموس، تشنج و وضعیت دکورتیکه در بیمار روی میدهند و سرانجام کوری، عدم تکلم و عدم پاسخ بروز میکند.
نقص آنزیم[ویرایش]
نقص در آنریم آریل سولفاتاز A (سولفاتیداز)
توارث ژنتیکی[ویرایش]
اتوزوم مغلوب.
میزان بروز[ویرایش]
نادر.
روش تشخیص[ویرایش]
- مایع مغزی نخاعی: افزایش پروتئین.
- ادرار: افزایش سولفاتیدها.
- بررسی آنزیم: در فیبروبلاستها و گلبولهای سفید.
درمان[ویرایش]
درمان حمایتی است. پیوند مغز استخوان در دوره قبل از بروز علائم یا اوایل آن ممکن است مفید باشد. پیوند در انواع نوجوانی و بزرگسالی به ترتیب نتایج خوب و تاحدی مفید داشتهاست، اما برای نوع شیرخوارگی دیررس توصیه نمیشود. آزمون تشخیص قبل از تولد: بررسی آنزیم در آمنیوسیتهای کشت شده و نمونه پرز کوریونی. نکته: در نوع کاذب نقص آنزیم، میزان آنزیم طبیعی است، اما فعالکننده ساپوسینB که کوفاکتوری است که فعالیت آنزیم را چند برابر افزایش میدهد، فعالیت کمی دارد
ویروس ایدز دو بیماری ژنتیکی را درمان می کند
محققان موسسه درمان ژنتیکی سن رافائل واقع در ایتالیا به تازگی دریافتند که ویروسی که موجب بروز بیماری ایدز میشود، توانایی درمان دونوع بیماری ژنتیکی را دارد. محققان توانستند با استفاده از ویروس HIV، دونوع بیماری ژنتیکی موسوم به لوکودیستروفی و سندروم ویسکات آلدریچ را در ۶ کودک درمان کنند. این نوع درمان با استفاده از ویروس HIV کاملاً ایمن است.
محققان در این تحقیق ۶ کودک داوطلب را از سه سال قبل با استفاده از این ویروس تحت درمان قرار دادند و درحال حاضر وضعیت آنها کاملاً رضایتبخش است. ایده استفاده از ویروس HIV برای درمان این بیماریهای ژنتیکی در سال ۱۹۹۶ مطرح شد. هر دو این بیماری ها به دلیل یک اختلال ژنتیکی بروز می کند و در آن میزان یک پروتئین حیاتی در سنین کودکی کاهش چشمگیر پیدا می کند. در بیماری لوکو دیستروفی، سیستم عصبی بیمار تحت تاثیر قرار میگیرد و با گذشت زمان توانایی تشخیصی و برخی قابلیتهای ذهنی بیمار از بین میرود. پس از سالها تحقیق در لابراتوار، محققان ایتالیایی روشی را یافتند که در آن میتوانند این اختلال ژنتیکی را با استفاده از سلولهای بنیادین مغز استخوان بیمار درمان کنند.
در این روش ساختار ژنتیکی سلولهای بنیادین با استفاده از ویروس HIV اصلاح شده است و مجددا به بدن بیمار تزریق میشود تا پروتئینهای لازم را به اندامهای مختلف برساند. در سندروم ویسکات آلدریچ، سیستم ایمنی بدن تضعیف و بیمار مستعد ابتلا به انواع عفونتها و سرطان میشود. در این بیماری سلولهای خون مستقیما تحت تاثیر قرار میگیرد. برای درمان این بیماری نیز با استفاده از روش مشابهی، سلولهای بنیادین اصلاح شده به بدن بیمار وارد می شود و عملکرد سیستم ایمنی وی را تصحیح میکند. در این پروژه تحقیقاتی بیش از ۷۰ نفر از محققان برجسته شرکت داشتند و ۱۶ بیمار مورد درمان قرار گرفتند. البته تنها ۶ نفر از این بیماران به مدت کافی تحت درمان بودهاند و نتایج تحقیق نیز به وضعیت همین ۶ نفر اشاره دارد.
















